ISO 13485とISO 14971ー医療機器とISOによる標準化
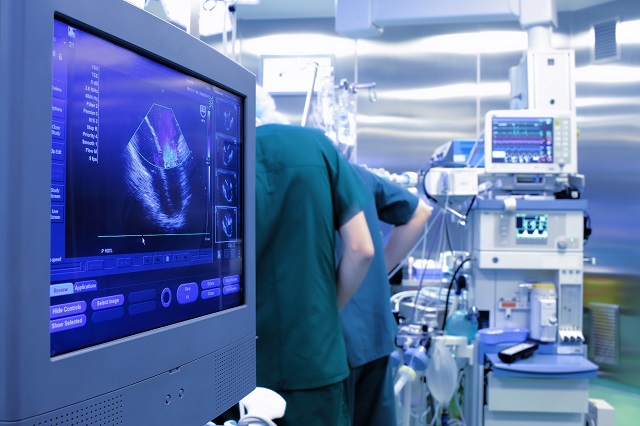
2005年5月、世界保健機構 (WHO) の医療機器規制国際整合化会議 (GHTF = global harmonization task force) の研究グループ1は、「医療機器 medical device」の定義について国際的な合意に達することに成功しました。この最初の定義は、その後、2012年5月に改訂され、ISOが採用しているのは、この改訂された2012年の定義です。
「医療機器 - 計器,器械,用具,機械,器具,埋込み用具,体外診断薬,ソフトウェア,材料又はその他の同類のもの若しくは関連する物質であって,単独使用又は組合せ使用かを問わず,製造業者が人体への使用を意図し,その使用目的が次の一つ以上であるもの。
- 疾病の診断,予防,監視,治療又は緩和
- 負傷の診断,監視,治療,緩和又は補助
- 解剖学的又は生理学的なプロセスの検査,代替,修復又は支援
- 生命支援又は維持
- 受胎調整
- 医療機器の消毒
- 人体から採取される標本の体外試験法による情報提供
さらに,薬学,免疫学又は新陳代謝の手段によって,体内又は体表において意図するその主機能を達成することはないものである。しかし,それらの手段によって意図する機能の実現が補助されてもよい」
このように広範な定義ですから、基本的な手技の用具から、複雑なコンピュータ制御の機械まで、医療機器のカタログが実に広範囲であるのは驚くに当たりません。医療機器には、傷口を覆うための包材やメスのようにシンプルな機器、車椅子や歯科用の椅子などの耐久機器、心臓用のペースメーカーやモニターをはじめ、義肢や人工関節などの埋め込み型の機器、人工呼吸器や肺換気装置などの生命維持用の機器、コンピュータ断層撮影 (CT) 用のスキャナーや核磁気共鳴画像 (MRI) の機械など最先端のソフトウェア制御の機器、体外診断薬や検査キットなどが含まれます。
健康と、健康でも怪我/疾病や障碍があってもその人なりの健康的な生活を守り、維持するための医療機器でもっとも重要なのは、意図した目的に対して安全な製品を一貫して設計し、開発し、製造し、設置し、配送することが最優先されるということです。医療機器にはこのような保証が必要なため、時の経過とともに国内及び国際的な規則、規制及び指令がたくさんできましたが、すべて医療機器の製造、供給およびサポートの側面を管理することを目的としています。
現在、GHTFは国際医療機器規制当局フォーラム (IMDRF = International Medical Device Regulators Forum) となり、国際的な医療機器の規制をさらに整合させ、合致させていこうとしています。日本はIMDRFのマネジメント委員会の10の参加国のうちの1つであり、独立行政法人医薬品医療機器総合機構 (PMDA = Pharmaceuticals and Medical Devices Agency) と厚生労働省からIMDRFの会合に代表を送り出しています。
ISO 13485
GHTFとIMDRF が推し進める整合、合致の作業と並行して、ISO の13485「医療機器 – 品質マネジメントシステム – 規制目的のための要求事項」が開発されました。ISO 13485は国際的に合意された規格であり、1996年に初版が発行され、その後2003年と2016年に改訂されました。この規格は医療機器業界特有の品質マネジメントシステムの要求事項を規定しています。ISO 13485はISO 9001の2008年版に基づいていますが、独立した規格ですから、ISO 13485の認証をもつ組織は、それだけではISO 9001に適合していると主張することはできません。なぜならISO 13485はISO 9001の要求事項全部に対応するものではないからです。
しかし、ISO 13485は製品及び技術的支援サービスの設計及び開発から解体及び廃棄まで、医療機器のライフサイクルのすべての段階をカバーしており、経営者の責任、資源のマネジメント、製品実現、並びに測定、分析及び改善に関する要求事項が中心に置かれています。
健康は、すべての国家にとって変わらず重要な政策的検討事項であり、高齢化と、それに伴う慢性的な状態を考えると、ISO 13485の認証件数は増加するのが当然であると考えられるでしょう。しかしながら、最新のISO サーベイのデータ (2018年までのデータを含む) は反対の傾向を示し、ISO 13485の認証は調査対象のすべての規格の中でもっとも大きなパーセンテージの下落のあった規格の1つであり、2017年は15,840の認証件数だったものが、2018年には14,618件と -8%の下落が示されています。
ISO サーベイでは、フランス、ドイツ及びイタリアで強い伸びが示されており、日本は2% と控えめながら伸び (2017年は568件で、2018年は580件) を示しているのに対し、英国では33% (1084件から721件) の下落が示されています。グローバルな医療機器市場は2018 年の140億ドルから2023には200億ドルに成長すると予想されていることを考えると、これはユーザが認める規格の価値の程度を反映し、マルチサイト認証を忌避する傾向を表しているということでしょう。
ISO 14971
ISO 13485は、他のほとんどの主要なマネジメントシステム規格と同様に、何をしなければならないかを定めていますが、どのように行うかは示していません。そのような要求事項の1つに「組織は,製品実現におけるリスクマネジメントの一つ以上のプロセスを文書化する」というものがあります。どのようなリスクマネジメントのアプローチを使うべきかは規定しておらず、7.1項の注記で「更なる情報は,ISO 14971を参照」と示しています。
「ISO 14971 医療機器 – 医療機器へのリスクマネジメントの適用 Medical devices – Application of risk management to medical devices (前の版は 2007年版、最新版は2019年版)」は、SaMD (software as a medical device 医療機器としてのソフトウェア) や体外診断用 (IVD = in vitro diagnostic) の医療製品も含む医療機器に関連するリスクをマネジメントするための用語、原則及びプロセスを特定しています。
主として医療機器メーカーを対象とするこのISO 規格は、医療目的で使用される機器や設備の安全性を推進しています。ISO 14971は、患者、医療行為の実施者及びその他の人々の健康に関連するリスクのみならず、資産、設備及び環境にダメージを与える可能性についても対象としています。
構造の面から見てみると、ISO 14971はリスクマネジメント、リスク分析、リスク評価、リスク管理、残留リスクの評価、リスクマネジメントレビュー、製造及び製造後の活動に対する一般的な要求事項、附属書A – 要求事項の論理的根拠、附属書 B – 医療機器のリスクマネジメントプロセス、附属書 C – 基本的なリスク概念 (ハザード、事象、危険状態及び起こりうる危害の例) から成っています。
ISO 14971の最新版は第3版であり、2019年12月に発行されたこの版は2つの2007年版 (最初3月に発行され、その後9月に修正版が発行された) に置き換わるものです。この最新版では、医療機器メーカーが要求事項を満たすために行わなければならない段階に関する詳細な情報を含めることで、前の版の技術的な要求事項を明確にすることが意図されています。また、現在の市場ニーズを反映して新しくアップデートされた用語も含まれています。さらに、2007年版に含まれていたガイダンスは、ISO 14971と同時期に改訂された 技術報告書「 ISO/TR 24971 医療機器 – ISO 14971 の適用のための手引き Medical devices – Guidance on the application of ISO 14971」に移されました。
まとめ
ISO 13485 のリスクマネジメントの要求事項の実施に苦労している組織に対して、ISO 14971はリスクマネジメントプロセスのすべての段階をカバーする貴重なサポートを提供しています。
これらの規格を一緒に運用することは必須ではありませんが、一緒に運用することには明らかに利点があると言えます。